变应性真菌性鼻-鼻窦炎诊断与治疗
文章来源:重庆仁品医院发布时间:2022-01-19
变应性真菌性鼻-鼻窦炎(allergicfungalrhinosnusitis,AFRS)1981年首先由Mlar等描述,属于非侵袭性真菌性鼻-鼻窦炎。在临床上,嗜酸性粒细胞性黏蛋白性鼻-鼻窦炎与AFRS很难区分,均表现为鼻窦内黄褐色的过敏性黏蛋白或稠厚的黏液。也有学者建议把合并变应性支气管肺曲霉菌病者称为鼻支气管变应性真菌病综合征。
一、发病机制
AFRS的发病机制尚不明确,目前的研究支持igE介导的I型过敏反应和Ⅲ型过敏反应(免疫复合物型)介导的黏膜炎症是主要机制。真菌免疫治疗有效以及当上、下气道接触高暴露的真菌时症状会复发提示上述机制,还有发现血清总IgE和真菌特异性IgG及症状相一致,但有时也发现真菌特异性IE和鼻窦内真菌不一致。金葡菌超抗原在鼻息肉发病中的作用也提示超抗原机制在AFRS发病中可能起作用。AFRS还可以侵犯邻近鼻窦,导致鼻窦扩大,黏液囊肿形成,周围骨质侵蚀以及突眼、复视及视力丧失。Ⅱ型MHC与AFRS的相关性近来被发现,且HLADQB10301和HLA-DQB1“0302可能是AFRS发病的危险因素,提示天然免疫在AFRS发病中的作用。
二、诊断
Kuhn和Javer提出AFRS的主要临床诊断标准,是目前诊断AFRS的主要依据:
①针对真菌的I型超敏反应(特异性IgE介导,皮肤试验和/或血清学检查证实);
②鼻息肉;
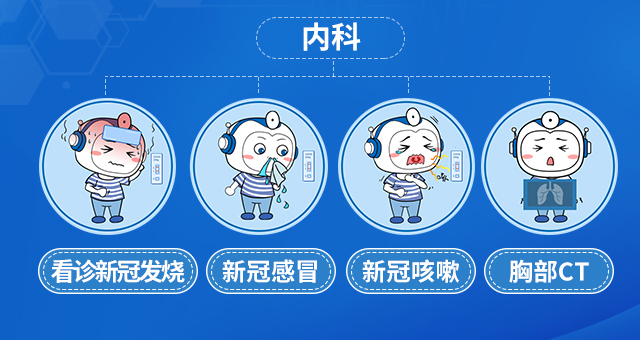
③特征性CT影像学表现窦腔扩大,窦腔内云絮状不规则高密度影(注:在软组织窗更明显)(图1);
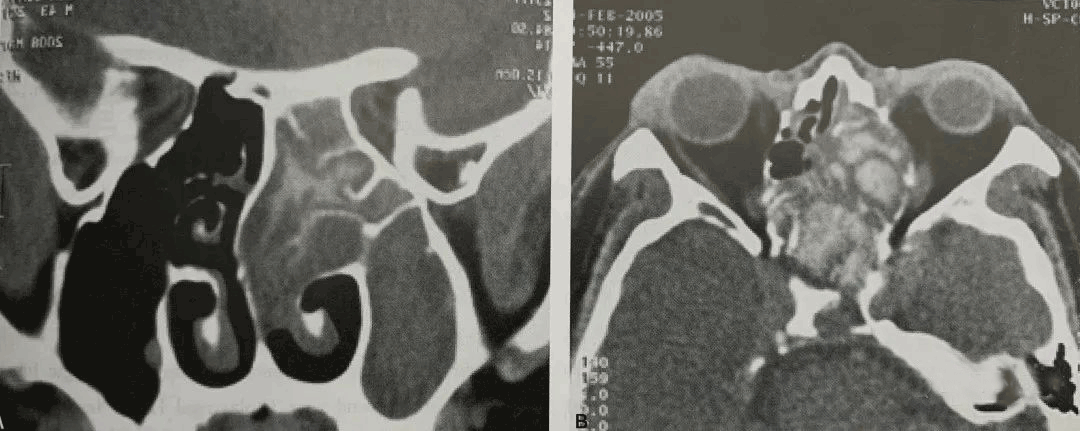
图1CT软组织窗显示左侧后组筛窦和上颌窦内可见絮状高密度影(左图),左侧后组筛窦和蝶窦内絮状高密度影(右图)
④嗜酸性粒细胞性黏蛋白(图2);
图2上窦口黄色高度黏稠的过敏性黏蛋白
⑤分泌物涂片真菌阳性。
次要诊断标准:
①哮喘;
②病变以单侧为主;
③CT表现骨质吸收;
④黏蛋白中可见Charcot-Leyden晶体(图3);
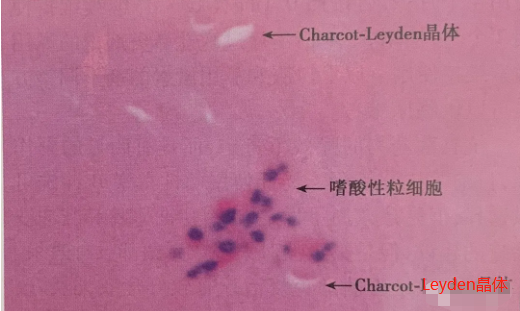
图3真菌性黏蛋白HE染色可见嗜酸性粒细胞和Charcot-Leyden
⑤分泌物培养真菌阳性;
⑥血液嗜酸性粒细胞增多。鼻窦MR也有一定的特征性表现,过敏性黏蛋白在T1加权增强像和T2加权像显示低信号或者信号缺失(图4)。
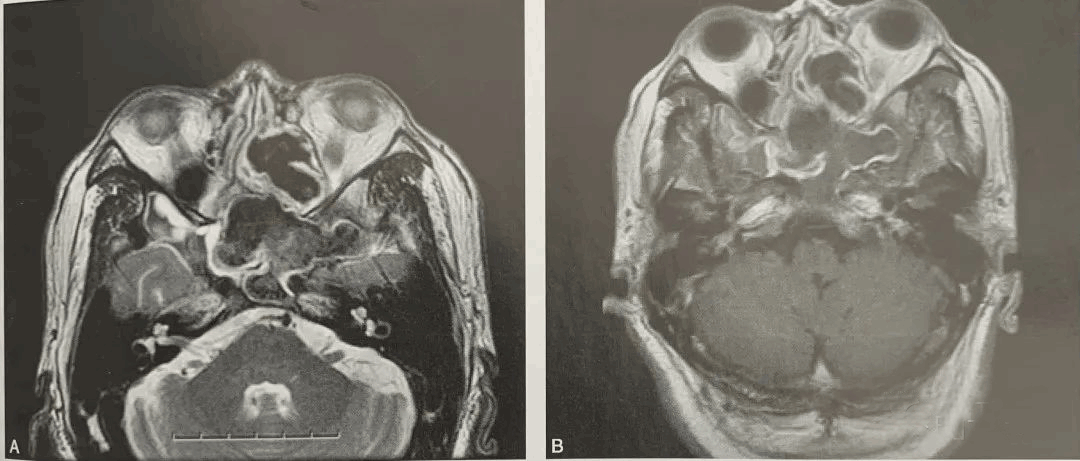
图4MRIT2加权像显示左侧后组筛窦和蝶窦黏膜长T2信号影,提示黏膜高度水肿,鼻窦中央部信号缺失或信号影(A),MRIT1加权增强像显示左侧后组筛窦和蝶窦黏膜增强信号影,提示黏膜血运丰富,鼻窦中央部信号缺失或混杂信号影(B)
但是需要指出的是,在诊断AFRS的时候一定要综合考虑以上诊断依据。由于真菌的过敏反应很常见,很多慢性鼻窦炎鼻息肉患者也合并真菌SPIs阳性,因此不能据此诊断为AFRS。诊断AFRS首先要有典型的临床表现,特别是在鼻窦内可见花生酱样的极度黏稠的过敏性黏蛋白,区别于真菌球性鼻窦炎的真菌团块;结合典型的CT和MRI影像学表现,提示AFRS。为了进一步明确是否有致病真菌所致的过敏反应,必须结合真菌SPIs、血清总IgE和特异性IgE检测结果,据此证实是真菌性过敏反应。作为病原学诊断,通过黏蛋白涂片发现真菌菌丝和孢子以及分泌物培养真菌阳性,目的是明确真菌种类,有条件的实验室还可以采用分子生物学方法鉴定黏蛋白中是否真菌以及真菌种类。为了鉴定嗜酸性粒细胞性黏蛋白,通过黏蛋白病理学染色发现黏蛋白中是否有Charcot-Leyden晶体以及真菌菌丝和孢子,综合以上几点来确诊AFS。有文献报道多例AFRS,但是其中部分病例实际是真菌球性鼻窦炎,反映了在临床上诊断中存在因为证据不足导致误诊的情况。而真菌球性鼻窦炎表现为窦腔内黄褐色到灰黑色的真菌团块,鼻窦CT表现为受累的窦壁骨质增生,窦口骨质吸收,窦内常可见钙化影,与AFRS易于鉴别。
一些似AFRS综合征(AFRS-likesyndrome)患者可能早期没有发展到足够多的证据,例如fergusson于2000提出的嗜酸性粒细胞性黏蛋白性鼻鼻窦炎的概念,该报道中的患者可能就是AFRS-likesyndrome,如果对这些患者长期随访的话,也可能会发展为符合上述5项主要诊断标准。
三、治疗
AFRS的治疗主要包括手术治疗、药物治疗和免疫治疗。
手术治疗要求充分开放鼻窦,清除黏蛋白和鼻息肉等病变组织,恢复鼻窦引流。口服糖皮质激素的疗效比较确切,但是疗程较长,全身副作用较大,需要注意评估长期使用糖皮质激素的禁忌证。为了监控评价疗效,Kupferberg等提出了鼻黏膜的分级:
0级:未见黏膜水肿或过敏性黏蛋白;
1级:黏膜水肿伴或不伴过敏性黏蛋白;
2级:鼻息肉样水肿黏膜伴或不伴过敏性黏蛋白;
3级:息肉伴过敏性黏蛋白。
参照这个黏膜评价标准,有学者建议术后开始给予:
口服强的松40mg/d(0。4mg/kg)持续4天,然后每4天按照0。1mg/(kg:d)递减,减至20mg/d或0。2mg/(kgd),术后1个月减至0。2mg/(kg),在鼻窦黏膜维持在0级的条件下按此剂量维持使用4个月;然后按照0。1mg/(kg·d)继续维持使用2个月,换用3~4倍治疗过敏性鼻炎剂量的鼻用激素维持使用。以上口服和鼻用激素的剂量调整方案可以供临床参考。
抗真菌药物的疗效不肯定,而且有明显的副作用,目前不推荐使用。局部使用两性霉素B冲洗可供选择,但是疗效尚不肯定,也有伊曲康唑鼻腔冲洗治疗的建议,但是氟康唑对大多数真菌都没有效果。术后使用致敏真菌的免疫治疗有较好疗效,能够改善症状,减少甚至停用全身用糖皮质激素,但是术前采用免疫治疗有可能加重病情,可能和手术前鼻窦内的真菌负荷有关。目前国内缺乏标准化程度较高的真菌过敏原疫苗,限制了真菌免疫治疗的应用。